推薦新聞
-
供應成都市青花椒魚底料:川味麻香的靈魂密碼多少錢四川味小二食品科技供應
-
供應成都市必嘗之選多少錢四川味小二食品科技供應
-
供應成都市烤魚傳統與創新的味覺盛宴排名四川味小二食品科技供應
-
供應成都市樂山美食之旅:翹腳牛肉價格四川味小二食品科技供應
-
提供成都市讓紅燒雞翅更上一層樓!批發四川味小二食品科技供應
-
提供成都市貴州酸湯:解鎖西南飲食的酸爽靈魂價格四川味小二食品科技供應
-
提供成都市云南有什么底料供應鏈批發四川味小二食品科技供應
-
供應成都市牛油火鍋底料應用教學視頻(一比二兌鍋)直銷四川味小二食品科技供應
-
提供成都市四川家喻戶曉底料生產線廠家四川味小二食品科技供應
-
銷售成都市四川老火鍋底料供應鏈價格四川味小二食品科技供應
重組蛋白用宿主細胞蛋白(HCP)殘留檢測
來源:
發布時間:2025-08-25
湖州申科生物建立了專業化宿主細胞蛋白殘留檢測平臺,利用 ELISA 方法分析宿主細胞蛋白總量,嚴格把控CV差異和回收率結果,保證實驗結果真實性,開發的試劑盒或抗體具有靈敏度高、特異性強等特點。在技術服務方面,平臺提供兩類關鍵支撐:一是覆蓋多種宿主(包括CHO、E.coli,酵母等)的殘留HCP檢測服務,直接輸出蛋白殘留量及樣品回收率數據;二是配套的樣品適用性驗證體系,通過基質定量下限驗證、樣品稀釋度驗證、準確性驗證及精密度驗證(含重復性與中間精密度)等多維度檢測方案,結合完整的試劑盒性能報告,確保檢測結果的準確性與可溯源性,為生物制品工藝雜質控制提供可靠保障。
定制化宿主細胞蛋白殘留檢測試劑盒產生的HCP抗體特異性更好,能檢出高風險HCP。重組蛋白用宿主細胞蛋白(HCP)殘留檢測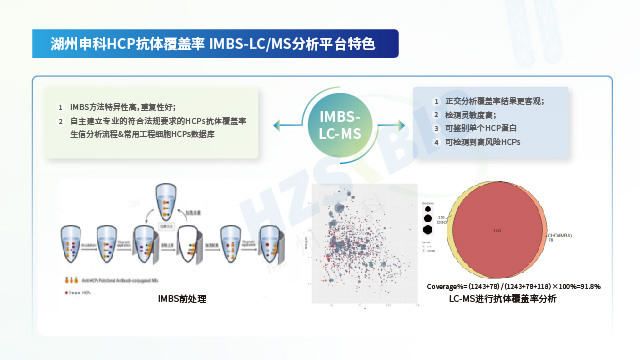
湖州申科生物推出的宿主細胞殘留蛋白檢測全自動 ELISA 分析系統,整合了標曲制備、樣本加樣、恒溫孵育、板孔清洗及結果檢測等全流程功能。系統搭載的高精度前處理模塊與檢測模塊,通準確控制實驗參數,有效減少人為操作誤差,確保實驗結果的穩定性與準確性。其多模塊單獨運行設計,可實現不同檢測任務的并行處理,大幅縮短實驗周期,明顯提升整體實驗效率。在保障結果可靠的基礎上,該系統實現了 ELISA 實驗的自動化操作、標準化流程與快速化輸出,降低了對實驗人員的技能要求,同時通過優化資源配置減少檢測成本。此外,系統內置完善的數據管理功能,可滿足實驗數據完整性記錄與全流程審計追蹤需求,嚴格符合 21 CFR Part 11 法規要求,并配備三級權限管理機制,進一步保障實驗數據的安全性與規范性。
上海工藝特異型宿主細胞蛋白(HCP)殘留檢測抗體制備湖州申科開發多種宿主 HCP 檢測試劑盒,提供抗體覆蓋率驗證服務。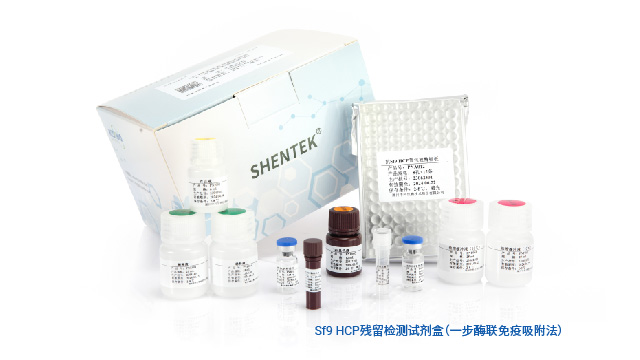
按照美國藥典1132章節的要求,HCPs校準品需滿足代表性要求,即能覆蓋實際工藝產品生產中的HCPs。從HCP免疫檢測方法使用目的和預期風險管理要求考慮,滿足工藝開發和驗證,同時為了應對下游工藝中潛在的異常工藝失效,或工藝變更需求,建議采用上游發酵工藝末端,如澄清處理后工藝點的樣本作為HCPs的來源。在實際制備中,可采用空細胞或空載細胞在模擬實際工藝的預定條件進行采集,通過二維電泳或高分辨率質譜等蛋白質組學方法進行模擬工藝和實際工藝下HCPs的代表性表征分析。越靠近下游HCPs蛋白種類越少,也越接近DS中HCPs,但是其可能無法滿足工藝開發和驗證需求,也無法保證工藝的潛在風險,往往不推薦使用,或只作為上游工藝HCPs免疫檢測法的輔助使用。
大腸埃希氏菌(Escherichia coli,E. coli)又稱大腸桿菌,其作為模式微生物被廣泛應用于生命科學研究中。隨著基因治療產業的大力發展,大腸桿菌也被主要應用于質粒DNA(pDNA)的生產。由于質粒樣品的常見提取工藝中往往使用條件劇烈的堿溶液進行細胞裂解和蛋白質變性,使得其中的HCPs與傳統物理破碎法獲得的HCPs有較大的差異,導致其在采用免疫學原理的檢測方法時,殘留檢測結果差別較大。湖州申科生物E.coli克隆菌堿裂HCP殘留檢測試劑盒用于大腸桿菌(又名大腸埃希菌)克隆菌株相關的HCPs檢測,如DH5α、Top10、JM109等。在抗體制備時采用堿裂工藝制備的HCPs免疫動物,獲得專門的抗體。適用于經堿液裂解工藝處理后的宿主細胞蛋白HCPs定量檢測。
遵循嚴格且科學的宿主細胞蛋白殘留檢測標準,是確保產品順利達標的重要基礎條件。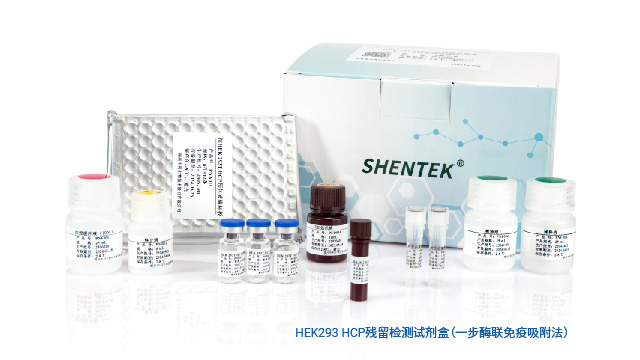
畢赤酵母(Pichia pastoris)是第二代酵母表達系統中的代表性菌株,是美國FDA認定的GRAS(Generally Recognized As Safe)微生物,具有表達水平高,產物活性好,培養成本低,易擴大為工業化生產等特點。在生物制藥領域,酶制劑、胰島素、表皮生長因子、膠原蛋白等多種生物制劑已經通過畢赤酵母系統進行商業化生產。與其他產品雜質一樣,畢赤酵母宿主殘留蛋白(HCP)可能對生物制品的安全性和有效性產生不利影響,因此在生產監測、產品放行等過程中需要對其進行定量研究并進行嚴格控制。SHENTEK®畢赤酵母HCP殘留檢測試劑盒(一步酶聯免疫吸附法)是湖州申科生物自主研發、具有完全自主知識產權的、實現關鍵試劑全國產化的畢赤酵母HCP通用檢測試劑盒。本試劑盒適用于基于GS115、X33等在內的畢赤酵母菌株生產的生物制品中宿主殘留蛋白的定量檢測,操作步驟少、快速,檢測專一性強,性能穩定可靠。
湖州申科HCP試劑盒定制化開發方案全流程按照ISO13485質量保證體系管理,符合審計要求。CHO宿主細胞蛋白(HCP)殘留檢測抗體覆蓋率驗證樣品與抗體的匹配程度對宿主細胞蛋白殘留檢測的結果影響很大。重組蛋白用宿主細胞蛋白(HCP)殘留檢測
MDCK(Madin-Darby Canine Kidney,馬丁達比犬腎上皮細胞)細胞系是一種來源于犬腎的長久性細胞系,其被普遍用作流感病毒增殖與純化、流感疫苗生產等過程中的細胞基質。基于其易感性、高產高滴度、無適應性突變、易馴化等優勢,MDCK細胞成為公認的適合于流感病毒毒株分離和流感疫苗生產的細胞系。與其他產品雜質一樣,MDCK宿主殘留蛋白(HCP)可能對生物制品的安全性和有效性產生不利影響,因此在生產監測、產品放行等過程中需要對其進行定量研究并進行嚴格控制。SHENTEK® MDCK HCP殘留檢測試劑盒(一步酶聯免疫吸附法)是湖州申科生物自主研發的、具有完全自主知識產權的、實現關鍵試劑全國產化的MDCK HCP通用檢測試劑盒。本試劑盒適用于基于MDCK細胞基質的病毒增殖及純化、疫苗生產等過程中MDCK宿主殘留蛋白的定量檢測。本試劑盒操作步驟少,快速,檢測專一性強,性能穩定可靠。
重組蛋白用宿主細胞蛋白(HCP)殘留檢測
相關新聞
- 重慶宿主細胞殘留DNA檢測銷售廠家 2025-09-16
- 單抗藥物用宿主細胞蛋白(HCP)殘留檢測橋接驗證 2025-09-16
- 浙江定制化宿主細胞蛋白(HCP)殘留檢測試劑盒開發要求 2025-09-16
- 上海生物制品宿主細胞殘留DNA檢測常用知識 2025-09-16
- 定制化宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-09-16
- 遼寧Human宿主細胞殘留DNA檢測生產企業 2025-09-16
- 四川E.coli宿主細胞殘留DNA檢測方案 2025-09-16
- 江蘇CHO宿主細胞殘留DNA檢測方案 2025-09-16
- 河南Vero宿主細胞殘留DNA檢測常見問題 2025-09-16
- 江蘇單抗藥物用宿主細胞蛋白(HCP)殘留檢測 2025-09-16
推薦新聞
- 天津定制玻璃儀器 2025-09-17
- 包含什么六字真言香囊費用 2025-09-17
- 北京進口葉綠素熒光成像系統 2025-09-17
- 佛山折疊拐杖 2025-09-17
- 河南無噪音護理墊/尿不濕粉碎處理機公司簡介 2025-09-17
- 重慶兒童矯形器裝配 2025-09-17
- 楊浦區本地教育軟件廠家電話 2025-09-17
- 浙江定制脊柱側彎支具型號 2025-09-17
- 山西糞便自動糞菌分離儀運用場景 2025-09-17
- 天津高純透明質酸酶常見問題 2025-09-17