釀酒酵母宿主細胞蛋白(HCP)殘留檢測高風險蛋白
來源:
發布時間:2025-08-29
影響宿主細胞蛋白(HCP)殘留檢測結果的因素之一是操作規范。一方面,實驗人員的專業技能和經驗對檢測結果的準確性有很大影響。熟練的實驗人員能夠準確地進行樣品處理、試劑配制和儀器操作,減少人為誤差。另一方面,一個合理的HCP檢測方法,在開發及應用時,應當考慮操作的合理變動區間(即耐用性)并設置相質控,從程序上盡量消除人為誤差對結果的影響。此外,嚴格遵循標準操作流程(SOP)是確保檢測結果可靠性的關鍵。操作步驟的不規范可能導致結果的重復性差或誤差增大。目前,湖州申科已正式推出全自動化HCP ELISA檢測系統,可以完成從樣品制備、孵育、洗板至數據采集等一系列操作,結合實驗室信息管理系統(LIMS),可以實現“輸入即輸出”,減少流程誤差。
篩選HCP試劑盒需考慮線性稀釋(一步法尤重)抗基質干擾穩定檢測值、批間一致性、工藝匹配性等因素。釀酒酵母宿主細胞蛋白(HCP)殘留檢測高風險蛋白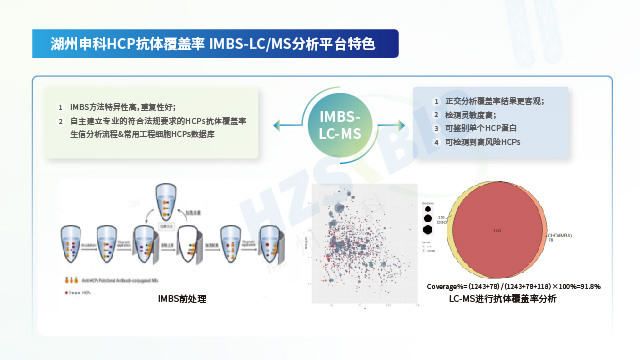
昆蟲細胞桿狀病毒表達系統(IC-BEVS)是以桿狀病毒作為外源基因載體,以昆蟲細胞作為宿主進行外源蛋白生產的真核表達系統。BVES具有易于規模化生產、培養成本低、生物安全性高等優勢,近年來陸續被研究用于生產重組蛋白、rAAV載體、亞單位疫苗(如病毒樣顆粒(VLP)疫苗)等, 在生物制品重組蛋白表達領域已有普遍運用。Sf9來源于草地夜蛾細胞系(Spodoptera frugiperda cell line,Sf),是目前較常用的昆蟲細胞系之一。SHENTEK® Sf9 HCP殘留蛋白檢測試劑盒(一步酶聯免疫吸附法),可定量檢測使用Sf9細胞系生產的生物制品中宿主細胞蛋白的殘留檢測。試劑盒抗體覆蓋率為70.4%-96.0%(IMBS-2D)和91.2% (IMBS-MS,Unique Peptide ≥2)。
MDCK宿主細胞蛋白(HCP)殘留檢測性能驗證HCP檢測方法驗證需評估線性范圍、中間精密度、靈敏度等關鍵參數。
為什么定制化試劑盒是宿主細胞蛋白殘留檢測的優先選擇?原因之一是建立定制化檢測體系,更滿足商業化生產HCP工藝雜質控制要求。在HCP校準品和HCP抗體兩大關鍵試劑組分滿足要求的前提下,定制化方法的建立和優化是基于真實純化中間品和原液樣品進行,通過優化檢測條件,提高對低濃度HCPs的檢測靈敏度,滿足工藝驗證和過程控制要求。在臨床三期,生產工藝需要進行系統驗證,以確保其穩定性和可重復性。定制化HCP ELISA檢測方法能夠更準確地監測生產工藝中HCP的去除效果,為工藝驗證提供有力支持。在過程控制中,通過工藝特異型的HCP ELISA檢測方法,可以實時監測生產過程中的HCP水平,具備更強的生產異常預警能力,及時發現生產風險,確保產品質量的穩定性。
影響宿主細胞蛋白(HCP)殘留檢測結果的因素之一是方法選擇。酶聯免疫吸附法(ELISA法)和液相色譜-質譜聯用方法(LC-MS法)是目前HCP檢測的兩大常用方法。文獻統計顯示,目前對于總HCP定量,ELISA仍是主流方法;MS法作為對特定蛋白(例如,高風險蛋白)的鑒定和定量,已成為重要的互補手段。此外檢測過程中使用的試劑和耗材的質量直接影響檢測結果的準確性。低質量的試劑可能導致假陽性或假陰性結果。例如,抗體的特異性和親和力不足,可能導致ELISA檢測中的交叉反應;抗原代表性不強或是抗體覆蓋率低,可能會導致漏檢;稀釋液抗干擾能力弱,可能影響檢測準確性。案例研究表明,采用定制化方法替代原有商業化試劑盒后,抗原代表性和抗體覆蓋率明顯提高,HCP檢測值整體升高。
湖州申科搭建高分辨蛋白質譜技術平臺,結合IMBS技術,推出了IMBS-MS抗體覆蓋率評估方法。
湖州申科生物依托高分辨質譜技術推出宿主細胞蛋白定制化檢測服務組合,覆蓋生物制品殘留蛋白分析需求。該平臺提供四類服務:HCP蛋白檢測定制化服務;通過ELISA、雙向電泳(2D)及LC-MS/MS技術,支持常規生物制品檢測、高危及工藝相關蛋白數據庫構建以及特殊生物制品分析;抗體覆蓋率服務采用自主研發的IMBS技術結合質譜,準確評估ELISA試劑盒對工程細胞HCP的捕獲能力,并完成校準品表征;靶向HCP檢測專注于高風險殘留蛋白的方法開發;同時提供蛋白種屬鑒定服務,利用LC-MS技術溯源樣品中的物種特異性肽段。該服務體系通過多技術聯用與深度定制化策略,滿足從基礎篩查到工藝關鍵雜質監控的全維度需求。
宿主細胞蛋白(HCP)殘留檢測對保障生物制品安全性和有效性至關重要。MDCK宿主細胞蛋白(HCP)殘留檢測性能驗證宿主檢測方法替換需橋接驗證,確保新舊方法結果一致性與可比性。釀酒酵母宿主細胞蛋白(HCP)殘留檢測高風險蛋白
畢赤酵母(Pichia pastoris)是第二代酵母表達系統中的代表性菌株,是美國FDA認定的GRAS(Generally Recognized As Safe)微生物,具有表達水平高,產物活性好,培養成本低,易擴大為工業化生產等特點。在生物制藥領域,酶制劑、胰島素、表皮生長因子、膠原蛋白等多種生物制劑已經通過畢赤酵母系統進行商業化生產。與其他產品雜質一樣,畢赤酵母宿主殘留蛋白(HCP)可能對生物制品的安全性和有效性產生不利影響,因此在生產監測、產品放行等過程中需要對其進行定量研究并進行嚴格控制。SHENTEK®畢赤酵母HCP殘留檢測試劑盒(一步酶聯免疫吸附法)是湖州申科生物自主研發、具有完全自主知識產權的、實現關鍵試劑全國產化的畢赤酵母HCP通用檢測試劑盒。本試劑盒適用于基于GS115、X33等在內的畢赤酵母菌株生產的生物制品中宿主殘留蛋白的定量檢測,操作步驟少、快速,檢測專一性強,性能穩定可靠。
釀酒酵母宿主細胞蛋白(HCP)殘留檢測高風險蛋白
相關新聞
- 重慶宿主細胞殘留DNA檢測銷售廠家 2025-09-16
- 單抗藥物用宿主細胞蛋白(HCP)殘留檢測橋接驗證 2025-09-16
- 浙江定制化宿主細胞蛋白(HCP)殘留檢測試劑盒開發要求 2025-09-16
- 上海生物制品宿主細胞殘留DNA檢測常用知識 2025-09-16
- 定制化宿主細胞蛋白(HCP)殘留檢測抗體制備 2025-09-16
- 遼寧Human宿主細胞殘留DNA檢測生產企業 2025-09-16
- 四川E.coli宿主細胞殘留DNA檢測方案 2025-09-16
- 江蘇CHO宿主細胞殘留DNA檢測方案 2025-09-16
- 河南Vero宿主細胞殘留DNA檢測常見問題 2025-09-16
- 江蘇單抗藥物用宿主細胞蛋白(HCP)殘留檢測 2025-09-16
推薦新聞
- 揚州國產智能健康管理系統24小時服務 2025-09-17
- 貴陽一次性醫療針頭一站式制造 2025-09-17
- 天津在哪找面部項目儀器生產企業 2025-09-17
- 北京保持器成型片定制廠家 2025-09-17
- 人抗子宮內膜抗體試劑盒 2025-09-17
- 北京輪式助行器工廠直銷 2025-09-17
- 咽鼓管功能障礙需要中耳負壓治療儀推薦廠家 2025-09-17
- 北京二類械字號葵花商標怎么樣 2025-09-17
- 江西奧托博克1C60小腿假肢 2025-09-17
- 靜安區本地高韌性尼龍 2025-09-17